Структура периодической системы. Структура периодической системы менделеева
Периодический закон Д.И. Менделеева и периодическая система химических элементов имеет большое значение в развитии химии. Окунемся в 1871 год, когда профессор химии Д.И. Менделеев, методом многочисленных проб и ошибок, пришел к выводу, что «… свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса». Периодичность изменения свойств элементов возникает вследствие периодического повторения электронной конфигурации внешнего электронного слоя с увеличением заряда ядра.
Современная формулировка периодического закона
такова:
«свойства химических элементов (т.е. свойства и форма образуемых ими соединений) находятся в периодической зависимости от заряда ядра атомов химических элементов».
Преподавая химию, Менделеев понимал, что запоминание индивидуальных свойств каждого элемента, вызывает у студентов трудности. Он стал искать пути создания системного метода, чтобы облегчить запоминание свойств элементов. В результате появилась естественная таблица , позже она стала называться периодической .
Наша современная таблица очень похожа на менделеевскую. Рассмотрим ее подробнее.
Таблица Менделеева
Периодическая таблица Менделеева состоит из 8 групп и 7 периодов.
Вертикальные столбцы таблицы называют группами . Элементы, внутри каждой группы, обладают сходными химическими и физическими свойствами. Это объясняется тем, что элементы одной группы имеют сходные электронные конфигурации внешнего слоя, число электронов на котором равно номеру группы. При этом группа разделяется на главные и побочные подгруппы .
В Главные подгруппы входят элементы, у которых валентные электроны располагаются на внешних ns- и np- подуровнях. В Побочные подгруппы входят элементы, у которых валентные электроны располагаются на внешнем ns- подуровне и внутреннем (n — 1) d- подуровне (или (n — 2) f- подуровне).
Все элементы в периодической таблице , в зависимости от того, на каком подуровне (s-, p-, d- или f-) находятся валентные электроны классифицируются на: s- элементы (элементы главной подгруппы I и II групп), p- элементы (элементы главных подгрупп III — VII групп), d- элементы (элементы побочных подгрупп), f- элементы (лантаноиды, актиноиды).
Высшая валентность элемента (за исключением O, F, элементов подгруппы меди и восьмой группы) равна номеру группы, в которой он находится.
Для элементов главных и побочных подгрупп одинаковыми являются формулы высших оксидов (и их гидратов). В главных подгруппах состав водородных соединений являются одинаковыми, для элементов, находящихся в этой группе. Твердые гидриды образуют элементы главных подгрупп I — III групп, а IV — VII групп образуют а газообразные водородные соединения. Водородные соединения типа ЭН 4 – нейтральнее соединения, ЭН 3 – основания, Н 2 Э и НЭ — кислоты.
Горизонтальные ряды таблицы называют периодами . Элементы в периодах отличаются между собой, но общее у них то, что последние электроны находятся на одном энергетическом уровне (главное квантовое число n — одинаково).
Первый период отличается от других тем, что там находятся всего 2 элемента: водород H и гелий He.
Во втором периоде находятся 8 элементов (Li - Ne). Литий Li – щелочной металл начинает период, а замыкает его благородный газ неон Ne.
В третьем периоде, также как и во втором находятся 8 элементов (Na - Ar). Начинает период щелочной металл натрий Na, а замыкает его благородный газ аргон Ar.
В четвёртом периоде находятся 18 элементов (K - Kr) – Менделеев его обозначил как первый большой период. Начинается он также с щелочного металла Калий, а заканчивается инертным газом криптон Kr. В состав больших периодов входят переходные элементы (Sc - Zn) — d- элементы.
В пятом периоде, аналогично четвертому находятся 18 элементов (Rb - Xe) и структура его сходна с четвёртым. Начинается он также с щелочного металла рубидий Rb, а заканчивается инертным газом ксенон Xe. В состав больших периодов входят переходные элементы (Y - Cd) — d- элементы.
Шестой период состоит из 32 элементов (Cs - Rn). Кроме 10 d -элементов (La, Hf - Hg) в нем находится ряд из 14 f -элементов(лантаноиды)- Ce — Lu
Седьмой период не закончен. Он начинается с Франций Fr, можно предположить, что он будет содержать, также как и шестой период, 32 элемента, которые уже найдены (до элемента с Z = 118).
Интерактивная таблица Менделеева
Если посмотреть на периодическую таблицу Менделеева и провести воображаемую черту, начинающуюся у бора и заканчивающуюся между полонием и астатом, то все металлы будут находиться слева от черты, а неметаллы – справа. Элементы, непосредственно прилегающие к этой линии будут обладать свойствами как металлов, так и неметаллов. Их называют металлоидами или полуметаллами. Это бор, кремний, германий, мышьяк, сурьма, теллур и полоний.
Периодический закон
Менделеев дал следующую формулировку Периодического закона: «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Существует четыре основных периодических закономерности:
Правило октета
утверждает, что все элементы стремятся приобрести или потерять электрон, чтобы иметь восьмиэлектронную конфигурацию ближайшего благородного газа. Т.к. внешние s- и p-орбитали благородных газов полностью заполнены, то они являются самыми стабильными элементами.
Энергия ионизации
– это количество энергии, необходимое для отрыва электрона от атома. Согласно правилу октета, при движении по периодической таблице слева направо для отрыва электрона требуется больше энергии. Поэтому элементы с левой стороны таблицы стремятся потерять электрон, а с правой стороны – его приобрести. Самая высокая энергия ионизации у инертных газов. Энергия ионизации уменьшается при движении вниз по группе, т.к. у электронов низких энергетических уровней есть способность отталкивать электроны с более высоких энергетических уровней. Это явление названо эффектом экранирования
. Благодаря этому эффекту внешние электроны мене прочно связаны с ядром. Двигаясь по периоду энергия ионизации плавно увеличивается слева направо.

Сродство к электрону – изменение энергии при приобретении дополнительного электрона атомом вещества в газообразном состоянии. При движении по группе вниз сродство к электрону становится менее отрицательным вследствие эффекта экранирования.

Электроотрицательность — мера того, насколько сильно стремится притягивать к себе электроны связанного с ним другого атома. Электроотрицательность увеличивается при движении в периодической таблице слева направо и снизу вверх. При этом надо помнить, что благородные газы не имеют электроотрицательности. Таким образом, самый электроотрицательный элемент – фтор.

На основании этих понятий, рассмотрим как меняются свойства атомов и их соединений в таблице Менделеева.
Итак, в периодической зависимости находятся такие свойства атома, которые связанны с его электронной конфигурацией: атомный радиус, энергия ионизации, электроотрицательность.
Рассмотрим изменение свойств атомов и их соединений в зависимости от положения в периодической системе химических элементов .
Неметалличность атома увеличивается при движении в периодической таблице слева направо и снизу вверх . В связи с этим основные свойства оксидов уменьшаются, а кислотные свойства увеличиваются в том же порядке — при движении слева направо и снизу вверх. При этом кислотные свойства оксидов тем сильнее, чем больше степень окисления образующего его элемента
По периоду слева направо основные свойства гидроксидов ослабевают,по главным подгруппам сверху вниз сила оснований увеличивается. При этом, если металл может образовать несколько гидроксидов, то с увеличением степени окисления металла, основные свойства гидроксидов ослабевают.
По периоду слева направо увеличивается сила кислородосодержащих кислот. При движении сверху вниз в пределах одной группы сила кислородосодержащих кислот уменьшается. При этом сила кислоты увеличивается с увеличением степени окисления образующего кислоту элемента.
По периоду слева направо увеличивается сила бескислородных кислот. При движении сверху вниз в пределах одной группы сила бескислородных кислот увеличивается.
Категории ,Периоди ческая систе ма элеме нтов Д. И. Менделеева, естественная , являющаяся табличным (или др. графическим) выражением . Периодическая система элементов разработана Д. И. Менделеевым в 1869-1871.
История периодической системы элементов. Попытки систематизации предпринимались различными учёными в , Англии, США с 30-х годов 19 в. Менделеева - И. Дёберейнер, Ж. Дюма, французский химик А. Шанкуртуа, англ. химики У. Одлинг, Дж. Ньюлендс и др. установили существование групп элементов, сходных по химическим свойствам, так называемых «естественных групп» (например, «триады» Дёберейнера). Однако эти учёные не шли дальше установления частных закономерностей внутри групп. В 1864 Л. Мейер на данных об предложил таблицу, показывающую соотношение для нескольких характерных групп элементов. Теоретических сообщений из своей таблицы Мейер не сделал.
Прообразом научной периодической системы элементов явилась таблица «Опыт системы элементов, основанной на их и химическом сходстве», составленная Менделеевым 1 марта 1869 (рис. 1 ). На протяжении последующих двух лет автор совершенствовал эту таблицу, ввёл представления о группах, рядах и периодах элементов; сделал попытку оценить ёмкость малых и больших периодов, содержащих, по его мнению, соответственно по 7 и 17 элементов. В 1870 он назвал свою систему естественной, а в 1871 - периодической. Уже тогда структура периодической системы элементов приобрела во многом современные очертания (рис. 2 ).
Периодическая система элементов не сразу завоевала признание как фундаментальное научное обобщение; положение существенно изменилось лишь после открытия Ga, Sc, Ge и установления двухвалентности Be (он долгое время считался трёхвалентным). Тем не менее периодическая система элементов во многом представляла эмпирическое обобщение фактов, поскольку был неясен физический смысл периодического закона и отсутствовало объяснение причин периодического изменения свойств элементов в зависимости от возрастания . Поэтому вплоть до физического обоснования периодического закона и разработки теории периодической системы элементов многие факты не удавалось объяснить. Так, неожиданным явилось открытие в конце 19 в. , которые, казалось, не находили места в периодической системе элементов; эта трудность была устранена благодаря включению в периодическую систему элементов самостоятельной нулевой группы (впоследствии VIIIa-подгруппы). Открытие многих «радиоэлементов» в начале 20 в. привело к противоречию между необходимостью их размещения в периодической системе элементов и её структурой (для более чем 30 таких элементов было 7 «вакантных» мест в шестом и седьмом периодах). Это противоречие было преодолено в результате открытия . Наконец, величина () как параметра, определяющего свойства элементов, постепенно утрачивала своё значение.
Одна из главных причин невозможности объяснения физического смысла периодического закона и периодической системы элементов состояла в отсутствии теории строения (см. , Атомная физика). Поэтому важнейшей вехой на пути развития периодической системы элементов явилась планетарная модель , предложенная Э. Резерфордом (1911). На её основе голландский учёный А. ван ден Брук высказал предположение (1913), что элемента в периодической системе элементов ( Z) численно равен заряду ядра (в единицах элементарного заряда). Это было экспериментально подтверждено Г. Мозли (1913-14, см. Мозли закон). Так удалось установить, что периодичность изменения свойств элементов зависит от , а не от . В результате на научной основе была определена нижняя граница периодической системы элементов ( как элемент с минимальным Z = 1); точно оценено число элементов между и ; установлено, что «пробелы» в периодической системе элементов соответствуют неизвестным элементам с Z = 43, 61, 72, 75, 85, 87.
Оставался, однако, неясным вопрос о точном числе , и (что особенно важно) не были вскрыты причины периодического изменения свойств элементов в зависимости от Z. Эти причины были найдены в ходе дальнейшей разработки теории периодической системы элементов на основе квантовых представлений о строении (см. далее). Физическое обоснование периодического закона и открытие явления изотонии позволили научно определить понятие « » (« »). Прилагаемая периодическая система (см. илл. ) содержит современные значения элементов по углеродной шкале в соответствии с Международной таблицей 1973. В квадратных скобках приведены наиболее долгоживущих . Вместо наиболее устойчивых 99 Tc, 226 Ra, 231 Pa и 237 Np указаны этих , принятые (1969) Международной комиссией по .
Структура периодической системы элементов . Современная (1975) периодическая система элементов охватывает 106 ; из них все трансурановые (Z = 93-106), а также элементы с Z = 43 (Tc), 61 (Pm), 85 (At) и 87 (Fr) получены искусственно. За всю историю периодической системы элементов было предложено большое количество (нескольких сотен) вариантов её графического изображения, преимущественно в виде таблиц; известны изображения и в виде различных геометрических фигур (пространственных и плоскостных), аналитических кривых (например, ) и т.д. Наибольшее распространение получили три формы периодической системы элементов: короткая, предложенная Менделеевым (рис. 2 ) и получившая всеобщее признание (в современном виде она дана на илл. ); длинная (рис. 3 ); лестничная (рис. 4 ). Длинную форму также разрабатывал Менделеев, а в усовершенствованном виде она была предложена в 1905 А. Вернером. Лестничная форма предложена английским учёным Т. Бейли (1882), датским учёным Ю. Томсеном (1895) и усовершенствована Н. (1921). Каждая из трёх форм имеет достоинства и недостатки. Фундаментальным принципом построения периодической системы элементов является разделение всех на группы и периоды. Каждая группа в свою очередь подразделяется на главную (а) и побочную (б) подгруппы. В каждой подгруппе содержатся элементы, обладающие сходными химическими свойствами. Элементы а- и б-подгрупп в каждой группе, как правило, обнаруживают между собой определённое химическое сходство, главным образом в высших , которые, как правило, соответствуют номеру группы. Периодом называется совокупность элементов, начинающаяся и заканчивающаяся (особый случай - первый период); каждый период содержит строго определённое число элементов. Периодическая система элементов состоит из 8 групп и 7 периодов (седьмой пока не завершен).
Специфика первого периода в том, что он содержит всего 2 элемента: H и He. Место H в системе неоднозначно: поскольку он проявляет свойства, общие со и с , его помещают либо в Ia-, либо (предпочтительнее) в VIIa-подгруппу. - первый представитель VIIa-подгруппы (однако долгое время Не и все объединяли в самостоятельную нулевую группу).
Второй период (Li - Ne) содержит 8 элементов. Он начинается Li, единственная которого равна I. Затем идёт Be - , II. Металлический характер следующего элемента В выражен слабо ( III). Идущий за ним C - типичный , может быть как положительно, так и отрицательно четырёхвалентным. Последующие N, O, F и Ne - , причём только у N высшая V соответствует номеру группы; лишь в редких случаях проявляет положительную , а для F известна VI. Завершает период Ne.
Третий период (Na - Ar) также содержит 8 элементов, характер изменения свойств которых во многом аналогичен наблюдающемуся во втором периоде. Однако Mg, в отличие от Be, более металличен, равно как и Al по сравнению с В, хотя Al присуща . Si, Р, S, Cl, Ar - типичные , но все они (кроме Ar) проявляют высшие , равные номеру группы. Таким образом, в обоих периодах по мере увеличения Z наблюдается ослабление металлического и усиление неметаллического характера элементов. Менделеев называл элементы второго и третьего периодов (малых, по его терминологии) типическими. Существенно, что они принадлежат к числу наиболее распространённых в природе, а С, N и O являются наряду с H основными элементами органической материи (органогенами). Все элементы первых трёх периодов входят в подгруппы а.
По современной терминологии (см. далее), элементы этих периодов относятся к s-элементам (щелочные и щёлочноземельные ), составляющим Ia- и IIa-подгруппы (выделены на цветной таблице красным цветом), и р-элементам (В - Ne, At - Ar), входящим в IIIa - VIIIa-подгруппы (их символы выделены оранжевым цветом). Для элементов малых периодов с возрастанием сначала наблюдается уменьшение , а затем, когда число в наружной оболочке уже значительно возрастает, их взаимное отталкивание приводит к увеличению . Очередной максимум достигается в начале следующего периода на щелочном элементе. Примерно такая же закономерность характерна для .
Четвёртый период (K - Kr) содержит 18 элементов (первый большой период, по Менделееву). После K и щёлочноземельного Ca (s-элементы) следует ряд из десяти так называемых (Sc - Zn), или d-элементов (символы даны синим цветом), которые входят в подгруппы 6 соответствующих групп периодической системы элементов. Большинство (все они ) проявляет высшие , равные номеру группы. Исключение - триада Fe - Co - Ni, где два последних элемента максимально положительно трёхвалентны, а в определённых условиях известно в VI. Элементы, начиная с Ga и кончая Kr (р-элементы), принадлежат к подгруппам а, и характер изменения их свойств такой же, как и в соответствующих интервалах Z у элементов второго и третьего периодов. Установлено, что Kr способен образовывать (главным образом с F), но VIII для него неизвестна.
Пятый период (Rb - Xe) построен аналогично четвёртому; в нём также имеется вставка из 10 (Y - Cd), d-элементов. Специфические особенности периода: 1) в триаде Ru - Rh - Pd только проявляет VIII; 2) все элементы подгрупп а проявляют высшие , равные номеру группы, включая и Xe; 3) у I отмечаются слабые металлические свойства. Таким образом, характер изменения свойств по мере увеличения Z у элементов четвёртого и пятого периодов более сложен, поскольку металлические свойства сохраняются в большом интервале .
Шестой период (Cs - Rn) включает 32 элемента. В нём помимо 10 d-элементов (La, Hf - Hg) содержится совокупность из 14 f-элементов, от Ce до Lu (символы чёрного цвета). Элементы от La до Lu химически весьма сходны. В короткой форме периодической системы элементов включаются в La (поскольку их преобладающая III) и записываются отдельной строкой внизу таблицы. Этот приём несколько неудобен, поскольку 14 элементов оказываются как бы вне таблицы. Подобного недостатка лишены длинная и лестничная формы периодической системы элементов, хорошо отражающие специфику на фоне целостной структуры периодической системы элементов. Особенности периода: 1) в триаде Os - Ir - Pt только проявляет VIII; 2) At имеет более выраженный (по сравнению с 1) металлический характер; 3) Rn, по-видимому (его мало изучена), должен быть наиболее реакционноспособным из .
Седьмой период, начинающийся с Fr (Z = 87), также должен содержать 32 элемента, из которых пока известно 20 (до элемента с Z = 106). Fr и Ra - элементы соответственно Ia- и IIa -подгрупп (s-элементы), Ac - аналог элементов IIIб -подгруппы (d-элемент). Следующие 14 элементов, f-элементы (с Z от 90 до 103), составляют семейство . В короткой форме периодической системы элементов они занимают Ac и записываются отдельной строкой внизу таблицы, подобно , в отличие от которых характеризуются значительным разнообразием . В связи с этим в химическом отношении ряды и обнаруживают заметные различия. Изучение химической природы элементов с Z = 104 и Z = 105 показало, что эти элементы являются аналогами и соответственно, то есть d-элементами, и должны размещаться в IVб- и Vб-подгруппах. Членами б-подгрупп должны быть и последующие элементы до Z = 112, а далее (Z = 113-118) появятся р-элементы (IIIa - VIlla-подгруппы).
Теория периодической системы элементов. В основе теории периодической системы элементов лежит представление о специфических закономерностях построения электронных оболочек (слоев, уровней) и подоболочек (оболочек, подуровней) в по мере роста Z (см. , Атомная физика). Это представление было развито в 1913-21 с учётом характера изменения свойств в периодической системе элементов и результатов изучения их . выявил три существенные особенности формирования электронных конфигураций : 1) заполнение электронных оболочек (кроме оболочек, отвечающих значениям главного квантового числа n = 1 и 2) происходит не монотонно до полной их ёмкости, а прерывается появлением совокупностей , относящихся к оболочкам с большими значениями n; 2) сходные типы электронных конфигураций периодически повторяются; 3) границы периодов периодической системы элементов (за исключением первого и второго) не совпадают с границами последовательных электронных оболочек.
В обозначениях, принятых в атомной физике, реальная схема формирования электронных конфигураций по мере роста Z может быть в общем виде записана следующим образом:

Вертикальными чертами разделены периоды периодической системы элементов (их номера обозначены цифрами наверху); жирным шрифтом выделены подоболочки, которыми завершается построение оболочек с данным n. Под обозначениями подоболочек проставлены значения главного (n) и орбитального (l) квантовых чисел, характеризующие последовательно заполняющиеся подоболочки. В соответствии с ёмкость каждой электронной оболочки равна 2n 2 , а ёмкость каждой подоболочки - 2(2l + 1). Из вышеприведённой схемы легко определяются ёмкости последовательных периодов: 2, 8, 8, 18, 18, 32, 32... Каждый период начинается элементом, в которого появляется с новым значением n. Таким образом, периоды можно характеризовать как совокупности элементов, начинающиеся элементом со значением n, равным номеру периода, и l = 0 (ns 1 -элементы), и завершающиеся элементом с тем же n и l = 1 (np 6 -элементы); исключение - первый период, содержащий только ls-элементы. При этом к а-подгруппам принадлежат элементы, для которых n равно номеру периода, а l = 0 или 1, то есть происходит построение электронной оболочки с данным n. К б-подгруппам принадлежат элементы, в которых происходит достройка оболочек, остававшихся незавершёнными (в данном случае n меньше номера периода, а l = 2 или 3). Первый - третий периоды периодической системы элементов содержат только элементы а-подгрупп.
Приведённая реальная схема формирования электронных конфигураций не является безупречной, поскольку в ряде случаев чёткие границы между последовательно заполняющимися подоболочками нарушаются (например, после заполнения в Cs и Ba 6s-подоболочки в появляется не 4f-, а 5d-электрон, имеется 5d-электрон в Gd и т.д.). Кроме того, первоначально реальная схема не могла быть выведена из каких-либо фундаментальных физических представлений; такой вывод стал возможным благодаря применению к проблеме строения .
Типы конфигураций внешних электронных оболочек (на илл. конфигурации указаны) определяют основные особенности химического поведения элементов. Эти особенности являются специфическими для элементов а-подгрупп (s-и р-элементы), б-подгрупп (d-элементы) и f-семейств ( и ). Особый случай представляют собой элементы первого периода (H и He). Высокая химическая атомарного объясняется лёгкостью отщепления единственного ls-электрона, тогда как конфигурация (1s 2) является весьма прочной, что обусловливает его химическую инертность.
Поскольку у элементов а-подгрупп происходит заполнение внешних электронных оболочек (с n, равным номеру периода), то свойства элементов заметно меняются по мере роста Z. Так, во втором периоде Li (конфигурация 2s 1) - химически активный , легко теряющий валентный , a Be (2s 2) - также , но менее активный. Металлический характер следующего элемента B (2s 2 p) выражен слабо, а все последующие элементы второго периода, у которых происходит застройка 2р-подоболочки, являются уже . Восьмиэлектронная конфигурация внешней электронной оболочки Ne (2s 2 p 6) чрезвычайно прочна, поэтому - . Аналогичный характер изменения свойств наблюдается у элементов третьего периода и у s-и р-элементов всех последующих периодов, однако ослабление связи внешних с ядром в а-подгруппах по мере роста Z определённым образом сказывается на их свойствах. Так, у s-элементов отмечается заметный рост химической , а у р-элементов - нарастание металлических свойств. В VIIIa-подгруппе ослабляется устойчивость конфигурации ns 2 np 6 , вследствие чего уже Kr (четвёртый период) приобретает способность вступать в . Специфика р-элементов 4-6-го периодов связана также с тем, что они отделены от s-элементов совокупностями элементов, в которых происходит застройка предшествующих электронных оболочек.
У переходных d-элементов б-подгрупп достраиваются незавершённые оболочки с n, на единицу меньшим номера периода. Конфигурация внешних оболочек у них, как правило, ns 2 . Поэтому все d-элементы являются . Аналогичная структура внешней оболочки d-элементов в каждом периоде приводит к тому, что изменение свойств d-элементов по мере роста Z не является резким и чёткое различие обнаруживается лишь в высших , в которых d-элементы проявляют определённое сходство с р-элементами соответствующих групп периодической системы элементов. Специфика элементов VIIIб-подгруппы объясняется тем, что их d-подоболочки близки к завершению, в связи с чем эти элементы не склонны (за исключением Ru и Os) проявлять высшие . У элементов Iб-подгруппы (Cu, Ag, Au) d-подоболочка фактически оказывается завершенной, но ещё недостаточно стабилизированной, эти элементы проявляют и более высокие (до III в случае Au).
Значение периодической системы элементов . Периодическая система элементов сыграла и продолжает играть огромную роль в развитии естествознания. Она явилась важнейшим достижением атомно-молекулярного учения, позволила дать современное определение понятия « » и уточнить понятия о и соединениях. Закономерности, вскрытые периодической системой элементов, оказали существенное влияние на разработку теории строения , способствовали объяснению явления изотонии. С периодической системой элементов связана строго научная постановка проблемы прогнозирования в , что проявилось как в предсказании существования неизвестных элементов и их свойств, так и в предсказании новых особенностей химического поведения уже открытых элементов. Периодическая система элементов - фундамент , в первую очередь неорганической; она существенно помогает решению задач синтеза с заранее заданными свойствами, разработке новых материалов, в частности полупроводниковых, подбору специфических для различных химических процессов и т.д. Периодическая система элементов- также научная основа преподавания .
Лит.: Менделеев Д. И., Периодический закон. Основные статьи, М., 1958; Кедров Б. М., Три аспекта атомистики. ч. 3. Закон Менделеева, М., 1969; Рабинович Е., Тило Э., Периодическая система элементов. История и теория, М.- Л., 1933; Карапетьянц М. Х., Дракин С. И., Строение , М., 1967; Астахов К. В., Современное состояние периодической системы Д. И. Менделеева, М., 1969; Кедров Б. М., Трифонов Д. Н., Закон периодичности и . Открытия и хронология, М., 1969; Сто лет периодического закона . Сборник статей, М., 1969; Сто лет периодического закона . Доклады на пленарных заседаниях, М., 1971; Spronsen J. W. van, The periodic system of chemical elements. A history of the first hundred years, Amst.- L.- N. Y., 1969; Клечковский В. М., Распределение атомных и правило последовательного заполнения (n + l)-групп, М., 1968; Трифонов Д. Н., О количественной интерпретации периодичности, М., 1971; Некрасов Б. В., Основы , т. 1-2, 3 изд., М., 1973; Кедров Б. М., Трифонов Д. Н., О современных проблемах периодической системы, М., 1974.
Д. Н. Трифонов.

Рис. 1. Таблица «Опыт системы элементов», основанной на их и химическом сходстве, составленная Д. И. Менделеевым 1 марта 1869.

Рис. 3. Длинная форма периодической системы элементов (современный вариант).

Рис. 4. Лестничная форма периодической системы элементов (по Н. , 1921).

Рис. 2. «Естественная система элементов» Д. И. Менделеева (короткая форма), опубликованная во 2-й части 1-го издания Основ в 1871.

Периодическая система элементов Д. И. Менделеева.
Периодическая система химических элементов — это классификация химических элементов, основанная на определенных особенностях строения атомов химических элементов. Она была составлена на основе Периодического закона, открытого в 1869 году Д. И. Менделеевым. В то время Периодическая система включала 63 химических элементов и по виду отличалась от современной. Сейчас в Периодической системы входят около ста двадцати химических элементов.
Периодическую систему составлен в виде таблицы, в которой химические элементы расположены в определенном порядке: по мере роста их атомных масс. Сейчас существует много видов изображения Периодической системы. Наиболее распространенным является изображение в виде таблицы с расположением элементов слева направо.
Все химические элементы в Периодической системе объединены в периоды и группы. Периодическая система включает семь периодов и восемь групп. Периодами называют горизонтальные ряды химических элементов, в которых свойства элементов изменяются от типичных металлических к неметаллическим. Вертикальные колонки химических элементов, которые содержат элементы, схожие по химическим свойствам, образуют группы химических элементов.
Первый, второй и третий периоды называют малыми, поскольку они содержат небольшое количество элементов (первый — два элемента, второй и третий — по восемь элементов). Элементы второго и третьего периодов называют типовыми, их свойства закономерно изменяются от типичного металла до инертного газа.
Все остальные периоды называют большими (четвертый и пятый содержат по 18 элементов, шестой — 32 и седьмой — 24 элемента). Особое сходство свойств проявляют элементы, находящиеся внутри больших периодов, в конце каждого четного ряда. Это так называемые триады: Ферум — Кобальт — Никол, образующих семью железа, и две другие: Рутений — Родий — Палладий и Осмий — Иридий — Платина, которые образуют семью платиновых металлов (платиноидов).
В нижней части таблицы Д. И. Менделеева расположены химические элементы, образующие семью лантаноидов и семью актиноидов. Все эти элементы формально входят в состав третьей группы и идут после химических элементов лантана (номер 57) и актиния (номер 89).
Периодическая система элементов содержит десять рядов. Малые периоды (первый, второй и третий) состоят из одного ряда, большие периоды (четвертый, пятый и шестой) содержат по два ряда каждый. В седьмом периоде находится один ряд.
Каждый большой период состоит из четного и нечетного рядов. В парных рядах содержатся элементы металлы, в нечетных рядах свойства элементов изменяются так, как в типовых элементов, т.е. от металлических до выраженных неметаллических.
Каждая группа таблицы Д. И. Менделеева состоит из двух подгрупп: главной и побочной. В состав главных подгрупп входят элементы как малых, так и больших периодов, то есть главные подгруппы начинаются либо с первого, или второго периода. В состав побочных подгрупп входят элементы только больших периодов, т.е. побочные подгруппы начинаются лишь с четвертого периода.
Периодическая система химических элементов - естественная классификация химических элементов, которая является графическим (табличным) выражением периодического закона химических элементов. Структура её, во многом сходная с современной, разработана Д. И. Менделеевым на основе периодического закона в 1869-1871 гг.
Прообразом периодической системы был "Опыт системы элементов, основанной на их атомном весе и химическом родстве", составленный Д. И. Менделеевым 1 марта 1869 г. На протяжении двух лет учёный непрерывно совершенствовал "Опыт системы", ввёл представление о группах, рядах и периодах элементов. В результате структура периодической системы приобрела во многом современные очертания.
Важным для её эволюции стало понятие о месте элемента в системе, определяемом номерами группы и периода. Опираясь на это понятие, Менделеев пришёл к выводу, что необходимо изменить атомные массы некоторых элементов: урана, индия, церия и его спутников. Это было первое практическое применение периодической системы. Менделеев также впервые предсказал существование нескольких неизвестных элементов. Учёный описал важнейшие свойства экаалюминия (будущего галлия), экабора (скандия) и экасилиция (германия). Кроме того, он предсказал существование аналогов марганца (будущих технеция и рения), теллура (полония), иода (астата), цезия (франция), бария (радия), тантала (протактиния). Прогнозы учёного в отношении данных элементов носили общий характер, поскольку эти элементы располагались в малоизученных областях периодической системы.
Первые варианты периодической системы во многом представляли лишь эмпирическое обобщение. Ведь был неясен физический смысл периодического закона, отсутствовало объяснение причин периодического изменения свойств элементов в зависимости от возрастания атомных масс. В связи с этим оставались нерешёнными многие проблемы. Есть ли границы периодической системы? Можно ли определить точное количество существующих элементов? Оставалась неясной структура шестого периода - каково точное количество редкоземельных элементов. Было неизвестно, существуют ли ещё элементы между водородом и литием, какова структура первого периода. Поэтому вплоть до физического обоснования периодического закона и разработки теории периодической системы перед ней не раз возникали серьёзные трудности. Неожиданным было открытие в 1894-1898 гг. плеяды инертных газов, которым, казалось, не находилось места в периодической системе. Эта трудность была устранена благодаря идее включить в структуру периодической системы самостоятельную нулевую группу. Массовое открытие радиоэлементов на стыке XIX и XX вв. (к 1910 г. их число составляло около 40) привело к резкому противоречию между необходимостью их размещения в периодической системе и её сложившейся структурой. Для них было только 7 вакантных мест в шестом и седьмом периодах. Эта проблема была решена в результате установления правил сдвига и открытия изотопов.
Одна из главных причин невозможности объяснить физический смысл периодического закона и структуру периодической системы состояла в том, что было неизвестно, как построен атом. Важнейшей вехой на пути развития периодической системы явилось создание атомной модели Э. Резерфордом (1911). На её основе голландский учёный А. Ван ден Брук (1913) высказал предположение, что порядковый номер элемента в периодической системе численно равен заряду ядра его атома (Z). Это экспериментально подтвердил английский ученый Г. Мозли (1913). Периодический закон получил физическое обоснование: периодичность изменения свойств элементов стала рассматриваться в зависимости от Z-заряда ядра атома элемента, а не от атомной массы.
В результате структура периодической системы значительно упрочилась. Была определена нижняя граница системы. Это водород - элемент с минимальным Z = 1. Стало возможным точно оценить количество элементов между водородом и ураном. Были определены "пробелы" в периодической системе, соответствующие неизвестным элементам с Z = 43, 61, 72, 75, 85, 87. Однако оставались неясными вопросы о точном количестве редкоземельных элементов и, что особенно важно, не были вскрыты причины периодичности изменения свойств элементов в зависимости от Z.
Опираясь на сложившуюся структуру периодической системы и результаты изучения атомных спектров, датский учёный Н. Бор в 1918-1921 гг. развил представления о последовательности построения электронных оболочек и подоболочек в атомах. Учёный пришёл к выводу, что сходные типы электронных конфигураций атомов периодически повторяются. Таким образом, было показано, что периодичность изменения свойств химических элементов объясняется существованием периодичности в построении электронных оболочек и подоболочек атомов.

В настоящее время периодическая система охватывает 126 элементов. Из них все трансурановые элементы (Z = 93-107), а также элементы с Z = 43 (технеций), 61 (прометий), 85 (астат), 87 (франций) получены искусственно. За всю историю существования периодической системы было предложено большое количество (> 500) вариантов ее графического изображения, преимущественно в виде таблиц, а также в виде различных геометрических фигур (пространственных и плоскостных), аналитических кривых (спиралей и пр.) и т. д. Наибольшее распространение получили короткая, длинная и лестничная формы таблиц.
В настоящее время предпочтение отдается короткой.
Фундаментальным принципом построения периодической системы является её подразделение на группы и периоды. Менделеевское понятие рядов элементов ныне не употребляется, поскольку лишено физического смысла. Группы, в свою очередь, подразделяются на главную (а) и побочную (b) подгруппы. В каждой подгруппе содержатся элементы - химические аналоги. Элементы а- и b-подгрупп в большинстве групп также обнаруживают между собой определённое сходство, главным образом в высших степенях окисления, которые, как правило, равны номеру группы. Периодом называется совокупность элементов, которая начинается щелочным металлом и заканчивается инертным газом (особый случай - первый период). Каждый период содержит строго определённое количество элементов. Периодическая система состоит из восьми групп и восьми периодов.
Особенность первого периода заключается в том, что он содержит всего 2 элемента: водород и гелий. Место водорода в системе неоднозначно. Поскольку он проявляет свойства, общие со щелочными металлами и с галогенами, то его помещают либо в Iаα-, либо в VIIaα - подгруппу, причем последний вариант употребляется чаще. Гелий - первый представитель VIIIa - подгруппы. Долгое время гелий и все инертные газы выделяли в самостоятельную нулевую группу. Это положение потребовало пересмотра после синтеза химических соединений криптона, ксенона и радона. В результате инертные газы и элементы бывшей VIII группы (железо, кобальт, никель и платиновые металлы) были объединены в рамках одной группы. Этот вариант не безупречен, так как инертность гелия и неона не вызывает сомнений.
Второй период содержит 8 элементов. Он начинается щелочным металлом литием, единственная степень окисления которого +1. Далее следует бериллий (металл, степень окисления +2). Бор проявляет уже слабо выраженный металлический характер и является неметаллом (степень окисления +3). Следующий за бором углерод - типичный неметалл, который проявляет степень окисления как +4, так и -4. Азот, кислород, фтор и неон - все неметаллы, причём у азота высшая степень окисления +5 соответствует номеру группы; для фтора известна степень окисления +7. Инертный газ неон завершает период.
Третий период (натрий - аргон) также содержит 8 элементов. Характер изменения их свойств во многом аналогичен тому, который наблюдался для элементов второго периода. Но здесь есть и своя специфика. Так, магний в отличие от бериллия более металличен, так же как и алюминий по сравнению с бором. Кремний, фосфор, сера, хлор, аргон - всё это типичные неметаллы. И все они, кроме аргона, проявляют высшие степени окисления, равные номеру группы.
Как видим, в обоих периодах по мере увеличения Z наблюдается ослабление металлических и усиление неметаллических свойств элементов. Д. И. Менделеев называл элементы второго и третьего периодов (по его словам, малых) типическими. Элементы малых периодов принадлежат к числу самых распространённых в природе. Углерод, азот и кислород (наряду с водородом) - органогены, т.е. основные элементы органической материи.
Все элементы первого-третьего периодов размещаются в аα-подгруппах.
Четвёртый период (калий - криптон) содержит 18 элементов. По Менделееву, это первый большой период. После щелочного металла калия и щелочноземельного металла кальция следует ряд элементов, состоящий из 10 так называемых переходных металлов (скандий - цинк). Все они входят в b-подгруппы. Большинство переходных металлов проявляют высшие степени окисления, равные номеру группы, кроме железа, кобальта и никеля. Элементы, начиная с галлия и кончая криптоном, принадлежат к а-подгруппам. Криптон в отличие от предшествующих инертных газов может образовывать химические соединения.
Пятый период (рубидий - ксенон) по своему построению аналогичен четвёртому. В нём также содержится вставка из 10 переходных металлов (иттрий - кадмий). У элементов этого периода есть свои особенности. В триаде рутений - родий - палладий для рутения известны соединения, где он проявляет степень окисления +8. Все элементы а-подгрупп проявляют высшие степени окисления, равные номеру группы, исключая ксенон. Можно заметить, что особенности изменения свойств у элементов четвёртого и пятого периодов по мере роста Z имеют по сравнению со вторым и третьим периодами более сложный характер.
Шестой период (цезий - радон) включает 32 элемента. В этом периоде кроме 10 переходных металлов (лантан, гафний - ртуть) содержится ещё и совокупность из 14 лантаноидов - от церия до лютеция. Элементы от церия до лютеция химически очень похожи, и на этом основании их давно включают в семейство редкоземельных элементов. В короткой форме периодической системы ряд лантаноидов включают в клетку лантана и расшифровку этого ряда дают внизу таблицы.
В чём состоит специфика элементов шестого периода? В триаде осмий - иридий - платина для осмия известна степень окисления +8. Астат имеет достаточно выраженный металлический характер. Радон, по всей вероятности, обладает наибольшей реакционной способностью из всех инертных газов. К сожалению, из-за того, что он сильно радиоактивен, его химия мало изучена.
Седьмой период начинается с франция. Подобно шестому, он также должен содержит 32 элемента. Франций и радий соответственно являются элементами Iaα- и IIаα-подгрупп, актиний принадлежит к III b-подгруппе. Наиболее распространено представление о семействе актиноидов, которое включает элементы от тория до лоуренсия и аналогично лантаноидам. Расшифровка этого ряда элементов также дается внизу таблицы.
Теперь посмотрим, как изменяются свойства химических элементов в подгруппах периодической системы. Основная закономерность этого изменения заключается в усилении металлического характера элементов по мере роста Z. Особенно отчётливо эта закономерность проявляется в IIIаα- VIIaα-подгруппах. Для металлов Iaα-IIIаα-подгрупп наблюдается рост химической активности. У элементов IVаα - VIIaα-подгрупп по мере увеличения Z наблюдается ослабление химической активности элементов. У элементов b-подгрупп изменение химической активности более сложно.
Теория периодической системы была разработана Н. Бором и другими учёными в 20-х гг. XX в. и основана на реальной схеме формирования электронных конфигураций атомов. Согласно этой теории, по мере роста Z заполнение электронных оболочек и подоболочек в атомах элементов, входящих в периоды периодической системы, происходит в следующей последовательности:
Номера периодов
На основании теории периодической системы можно дать следующее определение периода: период есть совокупность элементов, начинающаяся элементом со значением n, равным номеру периода, и l = 0 (s-элементы) и заканчивающаяся элементом с тем же значением n и l = 1 (р-элементы). Исключение составляет первый период, содержащий только 1s-элементы. Из теории периодической системы следуют и числа элементов в периодах: 2, 8, 8, 18, 18, 32...
На приложенной цветной вкладке символы элементов каждого типа (s-, р-, d- и f-элементы) изображены на определённом цветовом фоне: s-элементы - на красном, р-элементы - на оранжевом, d-элементы - на синем, f-элементы - на зелёном. В каждой клетке приведены порядковые номера и атомные массы элементов, а также электронные конфигурации внешних электронных оболочек, которые в основном и определяют химические свойства элементов.
Из теории периодической системы следует, что к а-подгруппам принадлежат элементы с n, равным номеру периода, и l = 0 и 1. К b-подгруппам относятся те элементы, в атомах которых происходит достройка оболочек, ранее остававшихся незавершёнными. Именно поэтому первый, второй и третий периоды не содержат элементов b-подгрупп.
Структура периодической системы элементов тесно связана со строением атомов химических элементов. По мере роста Z периодически повторяются сходные типы конфигурации внешних электронных оболочек. А именно они определяют основные особенности химического поведения элементов. Эти особенности по-разному проявляются для элементов а-подгрупп (s- и р-элементы), для элементов b-подгрупп (переходные d-элементы) и элементов f-семейств - лантаноидов и актиноидов. Особый случай представляют элементы первого периода - водород и гелий. Для водорода характерна высокая химическая активность, потому что его единственный 1s-электрон легко отщепляется. В то же время конфигурация гелия (1s 2) весьма устойчива, что обусловливает его полную химическую бездеятельность.
У элементов а-подгрупп происходит заполнение внешних электронных оболочек (с n, равным номеру периода); поэтому свойства этих элементов заметно изменяются по мере роста Z. Так, во втором периоде литий (конфигурация 2s) - активный металл, легко теряющий единственный валентный электрон; бериллий (2s 2) - также металл, но менее активный вследствие того, что его внешние электроны более прочно связаны с ядром. Далее, бор (2s 2 р) имеет слабо выраженный металлический характер, а все последующие элементы второго периода, у которых происходит построение 2р-подоболочки, являются уже неметаллами. Восьмиэлектронная конфигурация внешней электронной оболочки неона (2s 2 р 6) - инертного газа - очень прочна.
Химические свойства элементов второго периода объясняются стремлением их атомов приобрести электронную конфигурацию ближайшего инертного газа (конфигурацию гелия - для элементов от лития до углерода или конфигурацию неона - для элементов от углерода до фтора). Вот почему, например, кислород не может проявлять высшей степени окисления, равной номеру группы: ведь ему легче достичь конфигурации неона путём приобретения дополнительных электронов. Такой же характер изменения свойств проявляется у элементов третьего периода и у s- и р-элементов всех последующих периодов. В то же время ослабление прочности связи внешних электронов с ядром в а-подгруппах по мере роста Z проявляется в свойствах соответствующих элементов. Так, для s-элементов отмечается заметный рост химической активности по мере роста Z, а для р-элементов - нарастание металлических свойств.
В атомах переходных d-элементов достраиваются не завершенные ранее оболочки со значением главного квантового числа n, на единицу меньшим номера периода. За отдельными исключениями, конфигурация внешних электронных оболочек атомов переходных элементов - ns 2 . Поэтому все d-элементы являются металлами, и именно поэтому изменения свойств d-элементов по мере роста Z не так резки, как мы это видели у s-и р-элементов. В высших степенях окисления d-элементы проявляют определенное сходство с р-элементами соответствующих групп периодической системы.
Особенности свойств элементов триад (VIII b-подгруппа) объясняются тем, что d-подоболочки близки к завершению. Вот почему железо, кобальт, никель и платиновые металлы, как правило, не склонны давать соединения высших степеней окисления. Исключение составляют лишь рутений и осмий, дающие оксиды RuO 4 и OsO 4 . У элементов Ib- и IIb-подгрупп d-подоболочка фактически оказывается завершенной. Поэтому они проявляют степени окисления, равные номеру группы.
В атомах лантаноидов и актиноидов (все они металлы) происходит достройка ранее не завершенных электронных оболочек со значением главного квантового числа n на две единицы меньше номера периода. В атомах этих элементов конфигурация внешней электронной оболочки (ns 2) сохраняется неизменной. В то же время f-электроны фактически не оказывают влияния на химические свойства. Вот почему лантаноиды так сходны.
У актиноидов дело обстоит гораздо сложнее. В интервале зарядов ядер Z = 90 - 95 электроны 6d и 5f могут принимать участие в химических взаимодействиях. А отсюда следует, что актиноиды проявляют гораздо более широкий диапазон степеней окисления. Например, для нептуния, плутония и америция известны соединения, где эти элементы выступают в семивалентном состоянии. Только у элементов, начиная с кюрия (Z = = 96), становится устойчивым трехвалентное состояние. Таким образом, свойства актиноидов значительно отличаются от свойств лантаноидов, и оба семейства поэтому нельзя считать подобными.
Семейство актиноидов заканчивается элементом с Z = 103 (лоуренсий). Оценка химических свойств курчатовия (Z = 104) и нильсбория (Z = 105) показывает, что эти элементы должны быть аналогами соответственно гафния и тантала. Поэтому ученые полагают, что после семейства актиноидов в атомах начинается систематическое заполнение 6d-подоболочки.
Конечное число элементов, которое охватывает периодическая система, неизвестно. Проблема её верхней границы - это, пожалуй, основная загадка периодической системы. Наиболее тяжёлый элемент, который удалось обнаружить в природе, - это плутоний (Z = 94). Достигнутый предел искусственного ядерного синтеза - элемент с порядковым номером 118. Остается открытым вопрос: удастся ли получить элементы с большими порядковыми номерами, какие и сколько? На него нельзя пока ответить сколь-либо определённо.
С помощью сложнейших расчетов, выполненных на электронных вычислительных машинах, ученые попытались определить строение атомов и оценить важнейшие свойства таких "сверхэлементов", вплоть до огромных порядковых номеров (Z = 172 и даже Z = 184). Полученные результаты оказались весьма неожиданными. Например, в атоме элемента с Z = 121 предполагается появление 8р-электрона; это после того, как в атомах c Z = 119 и 120 завершилось формирование 85-подоболочки. А ведь появление р-электронов вслед за s-электронами наблюдается только в атомах элементов второго и третьего периодов. Расчёты показывают также, что у элементов гипотетического восьмого периода заполнение электронных оболочек и подоболочек атомов происходит в очень сложной и своеобразной последовательности. Поэтому оценить свойства соответствующих элементов - проблема весьма сложная. Казалось бы, восьмой период должен содержать 50 элементов (Z = 119-168), но согласно расчетам, он должен завершаться у элемента с Z = 164, т. е. на 4 порядковых номера раньше. А "экзотический" девятый период, оказывается, должен состоять из 8 элементов. Вот его "электронная" запись: 9s 2 8p 4 9p 2 . Иными словами, он содержал бы всего 8 элементов, как второй и третий периоды.
Трудно сказать, насколько соответствовали бы истине расчёты, проделанные с помощью ЭВМ. Однако если бы они были подтверждены, то пришлось бы серьезно пересмотреть закономерности, лежащие в основе периодической системы элементов и её структуры.
Периодическая система сыграла и продолжает играть огромную роль в развитии различных областей естествознания. Она явилась важнейшим достижением атомно-молекулярного учения, способствовала появлению современного понятия "химический элемент" и уточнению понятий о простых веществах и соединениях.
Закономерности, вскрытые периодической системой, оказали существенное влияние на разработку теории строения атомов, открытие изотопов, появление представлений о ядерной периодичности. С периодической системой связана строго научная постановка проблемы прогнозирования в химии. Это проявилось в предсказании существования и свойств неизвестных элементов и новых особенностей химического поведения элементов, уже открытых. Ныне периодическая система представляет фундамент химии, в первую очередь неорганической, существенно помогая решению задачи химического синтеза веществ с заранее заданными свойствами, разработке новых полупроводниковых материалов, подбору специфических катализаторов для различных химических процессов и т.д. И наконец, периодическая система лежит в основе преподавания химии.
Как пользоваться таблицей Менделеева?Для непосвященного человека читать таблицу Менделеева – все равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева, между прочим, если ей правильно пользоваться, может рассказать о мире очень многое. Помимо того, что сослужит Вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов. Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов. При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.

Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств. Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.

В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически. Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
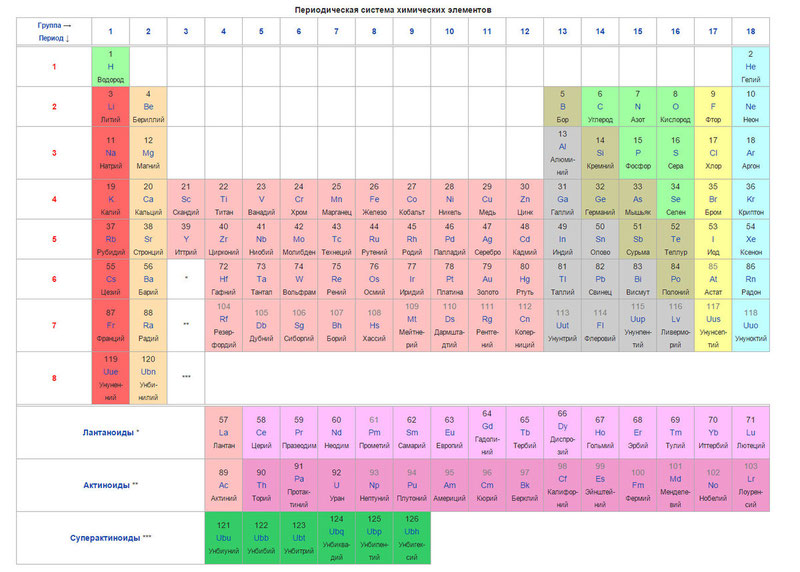
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.
- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваютс я.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.

Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы). Если округлить атомную массу до ближайшего целого, мы получим так называемое массовое число. Разность массового числа и атомного числа дает количество нейтронов в ядре. Так, число нейтронов в ядре гелия равно двум, а у лития – четырем.
Вот и закончился наш курс "Таблица Менделеева для чайников". В завершение, предлагаем Вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал Вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о , которые с радостью поделятся с Вами своими знаниями и опытом.






